RIFAXIMIN (XIFAXAN) ZUR PROPHYLAXE DER HEPATISCHEN ENZEPHALOPATHIE
Das Antibiotikum Rifaximin (XIFAXAN) wird seit April 2013 zur Rezidivprophylaxe der hepatischen Enzephalopathie angeboten.1 Bereits seit 2008 ist das Mittel bei unkomplizierter Reisediarrhö zugelassen (a-t 2008; 39: 121-3).2 Offenbar wird Rifaximin seit Längerem off label auch zur Akutbehandlung der hepatischen Enzephalopathie verwendet, wofür aber hinreichende Nutzenbelege fehlen.3
EIGENSCHAFTEN: Das schlecht absorbierbare Rifamycinderivat bindet an die Beta-Untereinheit der bakteriellen RNA-Polymerase und unterdrückt damit die bakterielle RNA-Synthese. Das Antibiotikum hat ein breites Wirkspektrum und hemmt unter anderem ammoniakbildende Darmbakterien. Dies soll bei Patienten mit schwer eingeschränkter Leberfunktion die Ammoniakexposition vermindern und so die Rezidivrate hepatischer Enzephalopathien senken (siehe Kasten Seite 50).1

WIRKSAMKEIT: Die Zulassung zur Rezidivprophylaxe der hepatischen Enzephalopathie beruht maßgeblich auf einer randomisierten doppelblinden Phase-III-Studie mit 299 im Mittel 56 Jahre alten Patienten mit Leberzirrhose, die im halben Jahr zuvor mindestens zwei Episoden einer hepatischen Enzephalopathie hatten.4,5 Ein Drittel der Teilnehmer hat weiterhin leichtgradige Symptome (Conn-Score* = 1).3 Ausgeschlossen sind unter anderem Patienten mit sehr schwerer Lebererkrankung (MELD-Score** > 25). Nur 9% der Studienteilnehmer haben einen MELD-Score über 18. Zu den Ausschlusskriterien gehören außerdem auslösende Faktoren einer hepatischen Enzephalopathie (siehe Kasten) in den letzten drei Monaten sowie Kreatininwerte über 2 mg/dl. Maximal sechs Monate lang nehmen die Patienten zweimal täglich 550 mg Rifaximin oder Plazebo und zu 90% begleitend Laktulose (BIFITERAL, Generika) ein. Primärer Endpunkt ist die Zeit bis zu einem Rezidiv, definiert als Anstieg des Conn-Scores auf mindestens zwei Punkte bzw. auf einen Punkt bei gleichzeitiger Zunahme des Flattertremors.5
Rezidive treten während der Beobachtungszeit in der Rifaximingruppe signifikant seltener auf (22,1% versus 45,9%, Hazard Ratio [HR] 0,42; 95% Konfidenzintervall [CI] 0,28-0,64), ebenso Krankenhausaufenthalte wegen oder kompliziert durch hepatische Enzephalopathie (13,6% vs. 22,6%; HR 0,5; 95% CI 0,29-0,87, sekundärer Endpunkt).5 Die Mortalität unterscheidet sich nicht (8,6% vs. 8,2% unter Plazebo).3
Das Wiederauftreten einer hepatischen Enzephalopathie wird nur bei einem Drittel der Patienten direkt durch die Studienärzte erhoben, ansonsten über Krankenhausaufnahmediagnosen, Berichte einer Pflegeperson oder per Telefon. Bei einem Rezidiv scheiden die Patienten aus der Studie aus, Dauer, Schweregrad und weiterer Verlauf werden nicht erfasst. Neben diesen methodischen Schwächen ist die Findung der Tagesdosis von 1.100 mg nicht nachvollziehbar.3
Die Wirksamkeit einer Monotherapie mit Rifaximin ist ungeklärt, da über 90% der Patienten gleichzeitig Laktulose einnehmen. Der präventive Nutzen des Disaccharids ist aber schlecht belegt (siehe Kasten). Auch fehlen kontrollierte Erfahrungen mit Rifaximin über sechs Monate hinaus. Für Patienten mit schwersten Lebererkrankungen, die besonders gefährdet sind, eine hepatische Enzephalopathie zu entwickeln, ist das Antibiotikum nicht geprüft. Dies gilt auch für Patienten mit schwereren Nierenfunktionseinschränkungen.
STÖRWIRKUNGEN: Insgesamt berichten je 80% der Patienten in beiden Vergleichsgruppen über Störwirkungen,5 unter Rifaximin dominieren periphere Ödeme (15% vs. 8% unter Laktulose allein), Schwindel (13% vs. 8%), Arthralgie (6% vs. 3%), Pruritus (9% vs. 6%), Anämie (8% vs. 4%) und Fieber (6% vs. 3%).1
Schwerwiegende unerwünschte Wirkungen, die häufiger unter Rifaximin auftreten, sind Ösophagusvarizen (2,9 % vs. 1,3%), Pneumonie (2,9% vs. 0,6%) und Anämie (2,9% vs. 0%).5 Zwei mit dem Antibiotikum behandelte Patienten erkranken an Clostridium-difficile-Kolitis gegenüber keinem unter Laktulose allein.3 In einer Extensionsstudie bzw. nach Markteinführung erkranken drei bzw. fünf weitere Patienten an der Darminfektion, einer stirbt.7 Auswirkungen der Langzeitbehandlung auf die Darmflora und Resistenzbildung sind bislang kaum untersucht.3
Der US-amerikanischen Arzneimittelbehörde FDA liegen Postmarketingberichte über exfoliative Dermatitis, angioneurotisches Ödem und anaphylaktische Reaktionen vor.7 Ein Fallbericht bringt eine toxische epidermale Nekrolyse mit der Einnahme von Rifaximin in Verbindung.8 In präklinischen Studien finden sich Zeichen von Hepatotoxizität, die die FDA auch angesichts einer bis zu 20-fach erhöhten Bioverfügbarkeit von Rifaximin bei zirrhotischen Patienten als bedenklich bewertet.9
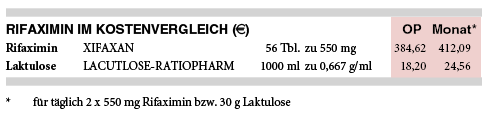
KOSTEN: Zweimal täglich 550 mg Rifaximin (XIFAXAN) kosten pro Monat 412 € und damit mehr als das 16-Fache einer Behandlung mit Laktulose-Sirup (z.B. LACTULOSE-RATIOPHARM Sirup; 25 € monatlich bei täglich 30 g Laktulose).
MEDIKAMENTÖSE PROPHYLAXE DER HEPATISCHEN ENZEPHALOPATHIE
Eine hepatische Enzephalopathie entsteht im Zuge einer schwer eingeschränkten Leberfunktion, die durch Leberzirrhose oder akutes Leberversagen bedingt sein kann, sowie bei portosystemischen Shunts. Die Pathogenese wird unter anderem damit erklärt, dass aus dem Darm aufgenommenes Ammoniak nicht entgiftet werden und so neurotoxisch wirken kann. Das klinische Bild reicht von leichten kognitiven Einschränkungen, die nur in psychometrischen Tests nachweisbar sind, über zeitliche Desorientierung, Persönlichkeitsveränderungen sowie motorische Dysfunktion bis hin zum Koma.1,2 Die Symptomatik kann stark fluktuieren und in rezidivierenden Episoden auftreten.1
Als auslösende Faktoren gelten unter anderem Infektionen, gastrointestinale Blutungen, Obstipation, Dehydratation, psychoaktive Medikamente, Elektrolytentgleisung und Nierenfunktionsstörung. Deren konsequente Behandlung bzw. Vermeidung steht laut einer internationalen Leitlinie von 2001 im Vordergrund von Therapie und Prophylaxe einer hepatischen Enzephalopathie.2 Eine medikamentöse Therapie zielt darauf, die Aufnahme von Ammoniak aus dem Darm zu vermindern. Nicht absorbierbare Disaccharide wie Laktulose (BIFITERAL, Generika) sollen das Darmmilieu ansäuern und damit sowohl ammoniakbildende Bakterien reduzieren als auch die Ammoniakabsorption direkt verringern.2,3 Laktulose wird zwar seit Jahrzehnten zur Behandlung der hepatischen Enzephalopathie eingesetzt, der Nutzen ist laut Cochrane-Metaanalyse von 2009 jedoch unzureichend belegt.5 Dies gilt auch für schlecht absorbierbare Antibiotika wie Neomycin (BYKOMYCIN, außer Handel), die die ammoniakproduzierenden Bakterien dezimieren sollen.5
Zur Prophylaxe einer hepatischen Enzephalopathie sind hierzulande nur Laktulose und das Antibiotikum Paromomycin (HUMATIN) zugelassen.3,4 Belege für den Nutzen von Paromomycin zur Prophylaxe finden wir nicht. In drei neueren randomisierten Studien6-8 senkt die prophylaktische Einnahme von Laktulose bei Patienten mit Leberzirrhose die Rate hepatischer Enzephalopathien im Vergleich zu keiner Medikation jeweils um etwa die Hälfte. Da die Studien offen durchgeführt sind und mit dem Conn-Score ein subjektives Endpunktkriterium haben, besteht das Risiko verzerrter Ergebnisse. Somit sehen wir in den gleichsinnigen Ergebnissen nur einen Hinweis auf einen Nutzen des Disaccharides zur Prophylaxe der hepatischen Enzephalopathie.
Angesichts mangelnder Alternativen und der erheblichen Beeinträchtigung durch eine hepatische Enzephalopathie erscheint uns neben der konsequenten Behandlung bzw. Vermeidung der auslösenden Faktoren die prophylaktische Einnahme von Laktulose bei diesen Patienten jedoch vertretbar. Nicht unterschätzt werden sollte dabei aber die Gefahr der Dehydratation, die wiederum eine hepatische Enzephalopathie auslösen kann.
| (R =randomisierte Studie, M = Metaanalyse) | |
| 1 | PRAKASH, R., MUELLEN, K.D.: Nat. Rev. Gastroenterol. Hepatol. 2010; 7: 515-25 |
| 2 | BLEI, A.T. et al.: Am. J. Gastroenterol. 2001; 96: 1968-76 |
| 3 | Abbott: Fachinformation BIFITERAL, Stand Juli 2012 |
| 4 | Pfizer: Fachinformation HUMATIN, Stand Juli 2012 |
| M 5 | ALS-NIELSEN, B. et al.: Nonabsorbable disaccharides for hepatic encephalopathy. Cochrane Database of Systematic Reviews, Stand Jan. 2009, Zugriff Juni 2013 |
| R 6 | SHARMA, B.C. et al.: Gastroenterol. 2009; 137: 885-91 |
| R 7 | AGRAWAL, A. et al.: Am. J. Gastroenterol. 2012; 107: 1043-50 |
| R 8 | SHARMA, P. et al.: J. Gastroenterol. Hepatol. 2012; 27: 1329-35 |
Das kaum absorbierbare Antibiotikum Rifaximin (XIFAXAN) ist seit einigen Wochen neben Reisedurchfall auch zur Rezidivprophylaxe einer hepatischen Enzephalopathie zugelassen.
Es senkt in einer Phase-III-Studie das Rezidivrisiko einer hepatischen Enzephalopathie gegenüber Plazebo um mehr als die Hälfte, wobei 90% der Patienten begleitend Laktulose (BIFITERAL, Generika) einnehmen. Auch Krankenhausaufenthalte im Zusammenhang mit hepatischer Enzephalopathie werden gemindert. Ein positiver Einfluss auf die Mortalität ist nicht belegt.
Die einzige vorliegende Studie hat Mängel. Die Dosisfindung ist nicht nachvollziehbar. Die Wirksamkeit als Monotherapie ist nicht untersucht. Kontrollierte Erfahrungen über sechs Monate hinaus fehlen.
Rifaximin ist bei Patienten mit schwersten Lebererkrankungen nicht geprüft.
Weitere Studien sind dringend erforderlich, um den Stellenwert des teuren Mittels bestimmen zu können. Derzeit kommt eine Anwendung von Rifaximin unseres Erachtens nur im Ausnahmefall in Betracht.
| (R =randomisierte Studie | |
| 1 | Norgine: Fachinformation XIFAXAN 550 mg, Stand Jan. 2013 |
| 2 | Norgine: Fachinformation XIFAXAN 200 mg, Stand Mai 2012 |
| 3 | FDA: Medical Review XIFAXAN, Stand 10. März 2010; http://www.access data.fda.gov/drugsatfda_docs/nda/2010/022554Orig1s000MedR.pdf |
| 4 | MHRA: Public Assessment Report TARGAXAN 550 mg, 29. Nov. 2012 http://www.mhra.gov.uk/home/groups/ par/documents/websiteresources/con249660.pdf |
| 5 | BASS, N.M. et al.: N. Engl. J. Med. 2010; 362: 1071-81 |
| 6 | WIESNER, R.H. et al.: Gastroenterology 2003; 124: 91-6 |
| 7 | FDA: GI Drugs Advisory Committee Meeting XIFAXAN, 23. Febr. 2010 http://www.fda.gov/downloads/ AdvisoryCommittees/CommitteesMeetingMaterials /Drugs/GastrointestinalDrugsAdvisory Committee/UCM203247.pdf |
| 8 | PATEL, A.S. et al.: Am. J. Health-Syst. Pharm. 2013; 70: 874-6 |
| 9 | FDA: Summary Review XIFAXAN, Stand 24. März 2010;
http://www.access data.fda.gov/drugsatfda_docs/nda/2010/022554Orig1s000SumR.pdf |
| * | Der Conn-Score teilt die hepatische Enzephalopathie in 5 klinische Stadien ein: 0 = keine Auffälligkeiten feststellbar; 1 = leichtes Aufmerksamkeitsdefizit, Angst; 2 = Lethargie, zeitliche Desorientierung, Persönlichkeitsveränderungen; 3 = Somnolenz, Verwirrtheit; 4 = Koma.4 |
| ** | MELD-Score: Der Model for End-Stage Liver Disease-Score zur Regelung der Organvergabe bei Lebertransplantation wird aus Bilirubin, Kreatinin und INR berechnet und dient zur Beurteilung der 3-Monats-Mortalität. In einer großen prospektiven Studie beträgt diese bei MELD-Score < 9: 2%, 10-19: 6%, 20-29: 20%, 30-39: 53% und > 40: 71%.6 |
© 2013 arznei-telegramm, publiziert am 7. Juni 2013
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
