In Europa leiden bis zu 3% der Männer und bis zu 0,6% der Frauen an Gicht.1 Eine asymptomatische Hyperurikämie mit
Harnsäurespiegeln über 7 mg/dl findet sich bei 20% der Männer und 3% der Frauen,2 die Mehrzahl der Betroffenen bleibt lebenslang
beschwerdefrei. Bei Männern beginnt Gicht meist zwischen dem 40. und 50. Lebensjahr, bei Frauen in der Regel erst nach den Wechseljahren. Die
Häufigkeit ist neben Alter und Geschlecht abhängig von Ernährungsgewohnheiten und genetischen Faktoren. Zu Diagnose und Therapie für
die seit Jahrhunderten bekannte Erkrankung sind erstaunlich wenige aussagekräftige Studien veröffentlicht.
Der Gicht liegt eine Störung des Purinstoffwechsels zu Grunde, die zum Anstieg der Harnsäure im Serum und zu Ablagerungen von
Harnsäurekristallen in Gelenken, Knochen, Weichteilen, Nieren und ableitenden Harnwegen führt. Purine werden mit der Nahrung zugeführt und
entstehen im Körper durch Abbau der DNA körpereigener Zellen sowie durch Neusynthese. Sie werden über Hypoxanthin und Xanthin zu
Harnsäure verstoffwechselt. Bei über 90% der erblich bedingten primären Formen der Gicht ist die Harnsäureausscheidung über die Nieren
vermindert.3 Selten liegen Enzymdefekte mit Überproduktion von Harnsäure vor (z.B. LESCH-NYHAN-Syndrom). Sekundäre
Hyperurikämien können bei verstärktem Zellumsatz auftreten (z.B. Tumorzerfall, Rhabdomyolyse, hämatopoetische Erkrankungen wie
Leukämie u.a.), bei Systemerkrankungen wie Psoriasis oder bei Niereninsuffizienz, Azidose, Einnahme von Diuretika u.a. Die Löslichkeitsgrenze für
Harnsäure beträgt bei 37 Grad Celsius im Plasma etwa 6,5 mg/dl, bei niedrigeren Temperaturen wie z.B. in den Extremitäten (30°C) fallen
Harnsäurekristalle bereits bei Werten von 5 mg/dl aus.4
Die Frage, ob Gicht oder Hyperurikämie einen eigenständigen Risikofaktor für kardiovaskuläre Erkrankungen darstellen, ist umstritten. In
neueren, validen Studien lässt sich kein Zusammenhang nachweisen.5,6
KLINIK UND VERLAUF: Bei den meisten Patienten manifestiert sich die Erkrankung erstmals mit einer plötzlich auftretenden äußerst
schmerzhaften Monoarthritis - dem akuten Gichtanfall.7 Er beginnt häufig in der Nacht und geht mit Rötung, Überwärmung
und Schwellung des Gelenks einher. Prinzipiell können alle Gelenke befallen sein, zu mehr als der Hälfte ist jedoch das Großzehengrundgelenk
betroffen, daneben Sprunggelenk, Knie- oder Mittelfußgelenk und seltener Finger-, Hand- oder Schultergelenk. Ein gleichzeitiger Befall mehrerer Gelenke betrifft
vorwiegend Frauen.4 Fieber und Leukozytose können vorkommen. Dem akuten Anfall gehen oft erhöhter Alkoholgenuss, opulentes Essen, aber
auch Fasten oder körperliche Anstrengung voraus. Die Symptomatik klingt auch unbehandelt nach sieben bis zehn Tagen ab.3 In der nachfolgenden
interkritischen Phase ist der Patient meist monate- oder sogar jahrelang beschwerdefrei. Einen erneuten Anfall erleiden 60% der Patienten innerhalb des ersten
Jahres.8 Die unbehandelte chronische Erkrankung geht mit häufigen Anfällen, irreversiblen Gelenkzerstörungen und
Uratablagerungen (Tophi) in Weichteilen, Sehnen und Knochen einher.
Nach Konsens in der Literatur wird Gicht auch bei klinischem Verdacht erst durch Nachweis von Uratkristallen in der Gelenkflüssigkeit oder in Tophi
gesichert.1,3,9 Durch diese Maßnahme können eine infektiöse Ursache als wichtigste Differenzialdiagnose ausgeschlossen werden, aber
auch weitere Erkrankungen, die wie Gicht zu dem Formenkreis der Kristallarthropathien (Pseudogicht [Chondrokalzinose] und Apatitkrankheit) gehören. Kann
die Diagnose nicht durch Punktion gesichert werden, können Kriterien der American Rheumatism Association herangezogen werden (vgl. Tabelle). In der
für die Erarbeitung der Kriterien zu Grunde liegenden Studie ergibt sich die höchste Diagnosewahrscheinlichkeit, wenn mindestens 6 der 11 Kriterien
zutreffen.10
Eine routinemäßige Gelenkpunktion wird im Praxisalltag in Deutschland bisher kaum durchgeführt, dagegen aber ein therapeutischer Effekt des
Extraktes der Herbstzeitlosen (Colchicin [COLCHICUM DISPERT u.a.]) als diagnostischer Beleg gewertet.2,11 Da Colchicin auch bei Pseudogicht zur
Linderung akuter Beschwerden verwendet wird, erscheint uns diese Methode der Diagnosesicherung wenig spezifisch.
Hyperurikämie ist für die Diagnosestellung nicht zwingend erforderlich. Gicht kann selten auch mit normalen Harnsäurespiegeln einhergehen. Das
Risiko eines Gichtanfalles steigt jedoch mit Dauer und Höhe der Hyperurikämie: Bei Harnsäurewerten über 9 mg/dl wird die jährliche
Inzidenz einer Gichtarthritis mit etwa 5% angegeben.4
BEHANDLUNG DES AKUTEN ANFALLS: Nichtsteroidale Antirheumatika (NSAR) gelten als Therapie der Wahl.1,3,4,12 Ein
besonderer Stellenwert einzelner Wirkstoffe lässt sich aus den wenigen kleinen kontrollierten Studien nicht ableiten. Diclofenac (DICLO 1A u.a.) und das bei
Gicht geprüfte Naproxen (PROXEN u.a.) erscheinen uns am besten begründet. Das bei Gicht ebenfalls untersuchte Indometazin (AMUNO u.a.) erachten
wir wegen seiner ausgeprägten zentralnervösen Störwirkungen wie Kopfschmerzen, Schwindel u.a. als Mittel der Reserve. Azetylsalizylsäure
(ASPIRIN u.a.) stört die Harnsäureausscheidung und ist somit kontraindiziert.1,13 Bekannte Störwirkungen von NSAR wie
gastrointestinale und renale Toxizität müssen insbesondere bei älteren und nieren- oder herzinsuffizienten Patienten beachtet werden.
Sind NSAR bei akutem Gichtanfall kontraindiziert oder unzureichend wirksam, werden alternativ Kortikoide wie Prednisolon (DECORTIN H u.a.)
verwendet.1,4,7 Die Diagnose muss gesichert und eine infektiöse Ursache ausgeschlossen sein. Trotz langjährigen Gebrauchs von Steroiden
finden wir nur eine unverblindete kontrollierte klinische Studie mit 20 Patienten, die keinen Vorteil von Triamcinolonacetonid (VOLON A) i.m. gegenüber NSAR
belegen kann.14 Lang wirkende Kortikoide wie Triamcinolon sind zur kurzfristigen Therapie bei akutem Gichtanfall ohnehin nicht angezeigt.
Intraartikuläre Steroide werden empfohlen, wenn höchstens ein bis zwei größere Gelenke betroffen sind.7,12 In einer
Beobachtungsstudie erhalten 19 Patienten mit gesicherter Diagnose je nach Größe des Gelenkes einmalig 8 mg bis 10 mg Triamcinolonacetonid
intraartikulär. Vollständige Beschwerdefreiheit wird für alle Patienten nach 48 Stunden angegeben.15 Wegen des potenziellen Risikos einer
septischen Arthritis nach intraartikulärer Kortikoidinjektion (vgl. a-t 1996; Nr. 4: 35-8) ist diese Maßnahme
unseres Erachtens jedoch nicht vertretbar.
Nach Ergebnissen einer kleinen randomisierten Studie kann eine mehrmals tägliche Kälteapplikation die medikamentöse Schmerzlinderung
unterstützen.16

Der aus Herbstzeitlosen gewonnene Colchicum-Extrakt wirkt entzündungshemmend. Er unterdrückt die Phagozytose von
Harnsäurekristallen durch Leukozyten. Colchicin hat keinen direkten analgetischen Effekt.3 Vergleichende Studien mit NSAR fehlen. Es existiert
unseres Wissens nur eine plazebokontrollierte Studie mit 43 Patienten. Maximal 6,5 mg Colchicin pro 24 Stunden lindern danach innerhalb von zwei Tagen bei
64%er Teilnehmer die Beschwerden um mindestens die Hälfte gegenüber 23% unter Plazebo. Alle Patienten der Verumgruppe klagen über Durchfall,
90% bereits vor Erreichen einer 50%igen Beschwerdereduktion.17
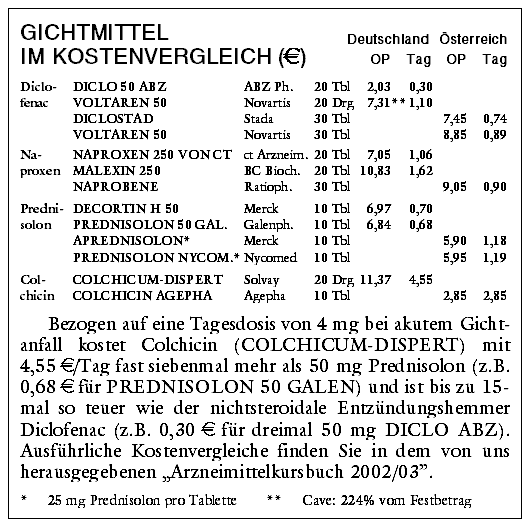
Empfohlen wird ein möglichst rascher Therapiebeginn mit initial 1 mg Colchicin oral, gefolgt von 0,5 mg alle zwei Stunden.17,18 Angaben zu
maximalen Tagesdosierungen reichen von 3 mg13 bis 8 mg,18 die Gesamtdosis von 12 mg pro Anfall darf nicht überschritten werden.18
Neben den bei bis zu 100%17 der Patienten beobachteten Magen-Darm-Störungen mit Erbrechen und Durchfall sind Benommenheit und
Myoneuropathien insbesondere bei langfristiger Einnahme häufig.18 Blutbildungsstörungen und Hemmung der Spermatogenese kommen vor.
Colchicin wird über CYP 3A4 metabolisiert,19 Interaktionen (z.B. mit Statinen) sind vorstellbar.
Bei akuter Vergiftung kommt es zu hämorrhagischer Enteritis, Übelkeit, Erbrechen und Durchfall. Die Patienten versterben an Herzversagen und
Atemlähmung. Todesfälle sind laut Fachinformation von COLCHICUM DISPERT bereits unter einer kumulativen Dosis von 8 mg pro Anfall beschrieben.
Schadwirkungen durch das "Mitosegift" wie aplastische Anämie u.a. können schon bei einer Gesamtdosis von 10 mg innerhalb weniger Tage
auftreten.18
Harnsäuresenkende Arzneimittel sind zur Behandlung eines akuten Anfalls kontraindiziert, da sie durch Änderung der
Serumharnsäurekonzentration einen Gichtanfall verlängern oder sogar auslösen können.12
 Die Studienlage zur medikamentösen Therapie der akuten Gicht ist
unbefriedigend: Valide Daten fehlen. Die Studienlage zur medikamentösen Therapie der akuten Gicht ist
unbefriedigend: Valide Daten fehlen.
 Bei akutem Gichtanfall erscheinen Diclofenac (DICLAC u.a.) sowie Naproxen
(PROXEN u.a.) als Mittel der Wahl. Sind nichtsteroidale Antirheumatika kontraindiziert oder wirkungslos, können kurzzeitig systemische Kortikoide (Prednisolon
u.a.) verwendet werden. Bei akutem Gichtanfall erscheinen Diclofenac (DICLAC u.a.) sowie Naproxen
(PROXEN u.a.) als Mittel der Wahl. Sind nichtsteroidale Antirheumatika kontraindiziert oder wirkungslos, können kurzzeitig systemische Kortikoide (Prednisolon
u.a.) verwendet werden.
 Colchicin (COLCHICUM DISPERT u.a.) erachten wir wegen schwerer
Störwirkungen als Mittel der Reserve bei sonst nicht zu beherrschendem Krankheitsverlauf. Colchicin (COLCHICUM DISPERT u.a.) erachten wir wegen schwerer
Störwirkungen als Mittel der Reserve bei sonst nicht zu beherrschendem Krankheitsverlauf.

|




